Albert Bourla anunțase la jumătatea lunii octombrie că se aștepta la dovezi de eficacitate asupra vaccinului dezvoltat de compania sa în parteneriat cu compania germană BioNTech până la sfârșitul lunii, după analiza primelor date din studiu clinic.
El a declarat marți într-o conferință telefonică că va avea aceste rezultate „în curând” și că le va împărtăși cu publicul larg după finalizarea anumitor sarcini administrative care ar dura aproximativ o săptămână.
Prin urmare, nu vor fi gata înainte de alegerile prezidențiale din 3 noiembrie.
„Să avem cu toții răbdarea necesară pentru acest lucru atât de important pentru sănătatea publică și economia globală”, a spus Bourla, subliniind că este „prudent optimist” cu privire la rezultatele testelor la vaccin.
Nu va fi oricum „nu un vaccin republican, sau un vaccin democrat, va fi un vaccin pentru cetățenii din întreaga lume”, a afirmat el.
Grupul încă intenționează să solicite autorizații de urgență de la agenția americană a medicamentelor, FDA, în a treia săptămână a lunii noiembrie.
Dacă organizația va da undă verde, Pfizer va putea furniza 40 de milioane de doze până la sfârșitul anului, a asigurat Bourla.
Laboratorul a declarat marți, cu ocazia publicării rezultatelor sale trimestriale, că a recrutat mai mult de 42.000 de participanți pentru studiul său clinic, dintre care 36.000 au primit deja o a doua doză pe 26 octombrie.
El vrea să testeze vaccinul pe 44.000 de persoane în total, mai mult decât cei 30.000 de participanți anticipați inițial.
Această extindere ar trebui să permită societății să crească diversitatea populațiilor testate, în special prin includerea minorilor și a pacienților cu boli cronice precum HIV sau hepatita C.
Pfizer este, cu Moderna, în pole position pentru a obține unda verde de la FDA.
Astrazeneca, în parteneriat cu Universitatea Britanică din Oxford, precum și Johnson & Johnson, au inițiat, de asemenea, studii de fază 3 în Statele Unite.
Pfizer va veni cu date despre vaccinul anti-COVID după alegerile prezidențiale din SUA
DE Andrei Vasilescu | Actualizat: 27.10.2020 - 22:20
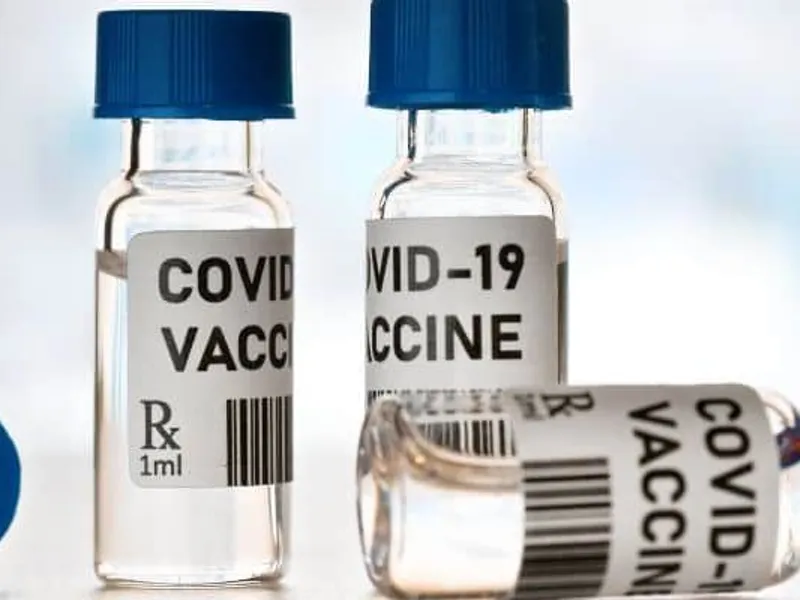
Nu va fi oricum „nu un vaccin republican, sau un vaccin democrat, va fi un vaccin pentru cetățenii din întreaga lume”, a afirmat CEO-ul Pfizer, Albert Bourla.
 Urmărește-ne pe Google News
Urmărește-ne pe Google News
 Digi Sport
Digi Sport
 Digi24
Digi24

Un cetățean american și soția sa spun că au fost reținuți și băgați în celule, fără nicio explicație, când se întorceau din Canada

Cum arată actorul din „Iisus din Nazareth”, la aproape 50 de ani de la premieră. Cum i-a schimbat viața interpretarea lui Hristos

O cercetătoare care a vorbit cu sute de centenari face 4 recomandări pentru o viață lungă și sănătoasă
 iAM SPORT
iAM SPORT

Istvan Kovacs, dialog UMILITOR cu Crețu, la FCSB - CFR! Cum poate să vorbească centralul cu jucătorii: 'Taci odată!'

A ”dispărut” după ce a denunțat blatul comis de echipa sa! Ce s-a ales de fostul jucător de la Rapid

”Anghel Iordănescu mi-a băgat mâna în gât și a spus că sunt dat afară”. Valentin Ceaușescu a salvat legenda Stelei '86
Mai multe articole din secțiunea
Sănătate

Care este simptomul banal care dă de gol apariția unui AVC? Peste 1000 de pacienți tineri l-au făcut

Atenție, părinți! Un medic explică efectele cocteilurilor de droguri luate de copiii de 14-16 ani

Pastila revoluționară pentru slăbit. Noul tratament a redus greutatea pacienților cu diabet cu 8%

Cazul medicilor decedați în mod misterios la Spitalul „Sf. Spiridon”: ITM Iași a demarat verificări
Altă moarte subită la Spitalul Sf. Spiridon, din Iaşi. Despre cine e vorba de data aceasta?

De la întuneric la lumină. O terapie revoluționară oferă unor copii orbi posibilitatea de a vedea
Comentarii
0
Trebuie să fii autentificat pentru a comenta!
Intră în contul tău
Crează cont nou
 Ultima oră
Ultima oră
 Tribuna politică
Tribuna politică
Textele publicate în această rubrică sunt advertoriale plătite conform Legii 334/2006 privind finanțarea activităților partidelor politice și a campaniilor electorale.
 Cele mai comentate
Cele mai comentate

Ce aparat din casă consumă cel mai mult când este oprit? Îți explodează factura la energie electrică
 Alege abonamentul care ți se potrivește
Alege abonamentul care ți se potrivește



 © 2025 NEWS INTERNATIONAL S.A.
© 2025 NEWS INTERNATIONAL S.A.










